الصفر المطلق وحالات جديدة للمادة

يَعرف الإنسان حتى وقت قريب ثلاث حالات للمادة؛ وهي الصلبة والسائلة والغازية، ثمّ ظهرت حالة رابعة للمادة وهي البلازما. ظلّ الاعتقاد بوجود أربع حالات للمادة فقط حتى بدأ العلماء في السباق للوصول للصّفر المطلَق فظهرت حالات جديدة للمادة تثير العجب.
علاقة الحرارة بحالات المادة:
عندما نسخّن المادة الصلبة فإنّ درجة حرارتها سترتفع، وعند درجة حرارة معينة يحدث الانصهار؛ أي تتحول المادة من الحالة الصلبة إلى الحالة السائلة. وإذا استمر التسخين فإنه عند درجة حرارة أخرى يحدث التبخّر وهو تحوُّل المادة من الحالة السائلة للحالة الغازية. وإذا استمرّ التسخين تصل المادة لحالة البلازما. ولفهم كيف تحدث هذه التحوّلات على المستوى الميكروسكوبي نذهب لزيارة الإلكترون الموجود في المجموعة القصصية للمهندس ياسر أبو الحسب “قبلة آينشتاين”. الإلكترون موجود في عيادة الطبيب النفسي: ندخل على الطبيب ونستأذنه في الحديث مع الإلكترون ونسأله:
أنا: هل من الممكن أن أسألك بعض الأسئلة؟
الإلكترون: بالرغم من عدم وجود وقت كافٍ لديّ لأنني سأعود لحجمي الذري مرة أخرى، تفضّل بالسؤال، ولكن سريعًا.
أنا: ما علاقة الحرارة بحالات المادة؟
الإلكترون: ما معنى الحرارة وما معنى حالات المادة؟
الطبيب: (موجّهًا كلامه لي) للإلكترون والأجسام الذرية داخل المادة رؤية مختلفة للتغيرات الفيزيائية تختلف عن التصوّرات التي نراها نحن.
أنا: شكرًا يا دكتور، سأراعي ذلك. (أمسكت قطعة من الثلج ووجهت كلامي للإلكترون.) أنا: كيف يكون شكل الجزيئات داخل هذه المادة؟
الإلكترون: تتراصّ على شكل كرات متجاورة ومرتبطة ببعضها البعض. تهتزّ هذه الجزيئات بطريقة دورانية حول نفسها.
أنا: وماذا يحدث عندما أزود هذه المادة بحرارة؟
الإلكترون: ماذا تعني بكلمة حرارة؟
الطبيب: يقصد ماذا يحدث إذا تمّ وضع المادة على النار؟
الإلكترون: يزداد اهتزاز جزيئات المادة.
الطبيب: بمعنى أنه كلما زادت الطاقة الحرارية تزداد جزيئات قطعة الثلج اهتزازًا.
الإلكترون: ولكن عند درجة معينة، وتمثّل درجة الصفر المئوية في حالة مكعّب الثلج نجد أنه بالرغم من تسخين المادة إلا أنّ اهتزاز الجزيئات لا يزيد وتظلّ الجزيئات بسرعتها لفترة.
الطبيب: عند هذه النقطة، بالنسبة لنا، نجد أنه بالرغم من تسخين قطعة الثلج تظل درجة حرارتها صفرًا، لا تتغير.
الإلكترون: (يكمل كلامه) خلال هذه الفترة نجد أن الروابط بين الجزيئات بدأت تضعف.
الطبيب: هذه هي حالة الانصهار، فعند نقطة الانصهار للماء وبسبب الحرارة الكامنة للانصهار بين جزيئات الماء نجد أنّ درجة حرارة الماء لا تتغير لوقت من الزمن بالرغم من إمدادها بطاقة حرارية، والسبب أنّ هذه الطاقة تضيع في تكسير الروابط بين جزيئات الماء لتتحوّل المادة بعدها للحالة السائلة. وبعدما يتحوّل الثلج للحالة السالة تمامًا تعود درجة حرارة المادة لترتفع بالنسبة لنا وتعود الجزيئات لتزيد سرعة اهتزازها بالنسبة للإلكترون.
أنا: آه، إذًا ما نراه نحن زيادةً في الحرارة تراه الأجسام الذرية زيادةً في سرعة اهتزاز الجزيئات. والعكس عندما تبرد المادة بالنسبة لنا، فبالنسبة للجزيئات يكون ذلك بطء في سرعة اهتزاز الجزيئات.
الإلكترون: وبعد تكسير الروابط نجد أنّ المسافات بين الجزيئات زادت، وكما ذكر الطبيب، تبدأ سرعة الجزيئات في الازدياد مرة أخرى حتى نصل لنقطة أخرى تتكسّر فيها كلّ الروابط تمامًا وتصبح الجزيئات حرّة الحركة بدون أية روابط. وعند هذه النقطة أيضًا تتوقف الزيادة في سرعة اهتزاز الجزيئات لفترة.
الطبيب: هذا يحدث عندما تتحول الحالة السائلة للحالة الغازية، وتسمّى نقطة التصعيد. وتتوقّف فيها درجة الحراة عن الازدياد لأنّ الطاقة الحرارية تصرف للتغلّب على الحرارة الكامنة للتصعيد. أي تُستخدَم لتكسير الروابط بين الجزيئات.
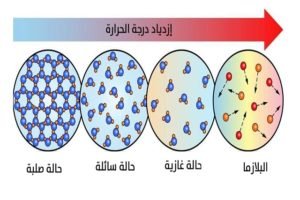
الإلكترون: وعند التسخين مرة أخرى تزيد سرعة اهتزاز الجزيئات حتى نصل لنقطة معينة أجد نفسي مع أصدقائي الإلكترونات مدفوعين خارج الذرة ونصبح أحرارًا.
أنا: نعم، هذه هي البلازما. فالإلكترونات التي تتحرّر سالبة الشحنة والذرات التي خرجت منها الإلكترونات تصبح موجبة الشحنة وتصبح المادة في حالة تأيُّن؛ تستجيب للمجالات الكهربية والمغناطيسية بالرغم من شكلها الغازي.
الإلكترون: لا يهمّني. ولكن أرجو أن تتركني مع الطبيب لأكمل له شكواي لأنّ الوقت يداهمني.
أنا: ولكن ما زال لدي سؤال. ماذا يحدث في الناحية المعاكسة؛ أي إذا تمّ تبريد المادة تحت درجة الصفر؟ وإلى أي درجة حرارة نستطيع تبريد المادة؟
الإلكترون: للأسف ليس لدي وقت…
أنا: إذًا شكرًا. (واستأذنتُ الطبيب للمغادرة لأواصل البحث عن ماذا يحدث للمادة عند تبريدها).
قانون شارل وصفر كلفن:
عاش العالم جاك شارل الفرنسي في الفترة من 1746م – 1823م. وانتُخب عضوًا في أكاديمية العلوم الفرنسية. اهتمّ بالغازات وصاغ قانون شارل عام 1787م، ويقول القانون:
إعلان
“عند ثبات الضغط يتغيّر حجم عيّنة من الغاز المثالي زيادة أو نقصانًا بطريقة طردية؛”
أي أنّ حجم الغاز يتناسب طرديًا مع درجة الحرارة، كلّما زادت درجة الحرارة يزيد حجم الغاز، والعكس. وسبب ذلك كما ذكرنا في مناقشتنا مع الإلكترون، في الحالة الغازية تصبح الجزيئات حرّة الحركة تمامًا، وكلّما زادت درجة الحرارة تزيد الطاقة الحركية للجزيئات وتبدأ في حركة عشوائية وهذا يسبّب تباعدًا بين الجزيئات ويزيد الحجم. ونلاحظ عمومًا أنه كلما قلّت درجة الحرارة فإنّ حجمها يقلّ، ولذلك نجد أنّ حجم عينة من المادة وهي في الحالة الصلبة أقل من حجمها وهي في الحالة السائلة.
بعد أن ظهر قانون شارل وانتشر في الأوساط العلمية، لاحظ اللورد كلفن أنّه عند رسم علاقة بيانية بين درجة الحرارة والحجم فإنها تكون على شكل خط مستقيم، وعند مدّ جميع الخطوط المستقيمة التي تمثّل الغازات المختلفة فإنها تصل لنفس درجة الحراة وهي 273.15 درجة تحت الصفر. وأُطلق عليها درجة الصفر المطلق، وقام ببناء تدريج لدرجة الحرارة على هذا الصفر وسمّاه “تدريج كلفن .

ما الذي يحدث للمادة عند الصفر المطلق؟ بالطبع لم يصل العلماء لدرجة الصفر المطلق إلى الآن. لأنّ الوصول لها يحتاج طاقةً لا نهائية. ونظريًا، تتوقّف حكّة الجزيئات تمامًا وتنكمش المادة تمامًا حتى تختفي، كما شرحنا سابقًا. ولكنّ الصفر المطلق ألهَم العلماء وبدأ سباقًا محمومًا للوصول لهذه الدرجة.
قام العالم مايكل فاراداي بإجراء تجارب أظهرت أنه تحت ضغط غازات الكلور والأمونيا تصبح سائلة، ونحن نعرف أنّ الكلور والأمونيا في درجة الحرارة العادية تكون غازية. وعند تبخير هذه السوائل الناتجة مرة أخرى تنخفض درجة حرارتهما بشكل مفاجئ. حاول فاراداي تطبيق هذه التجربة على جميع الغازات ولكن وجد أنّ هناك غازات كان يظنّ أنه لا يمكن أن تُسال مهما كانت الضغوط عليها، وسمّاها الغازات الثابتة (الهيدروجين – النيتروجين – الأكسجين)، وترك ميدان البحث في هذا المجال بعد أن وصل إلى درجة 130 درجة مئوية تحت الصفر أي 143 درجة كلفن. ونجد أنّ المسافة ما زالت كبيرة للوصول إلى الصفر كلفن (الصفر المطلَق) وبعد ثلاثين سنة مضت لم يستطع أحد أن يتخطى هذه الدرجة. أصبح التحدي هو تسييل الغازات الثابتة التي كان يظنّ فاراداي استحالة تسييلها. قام الفيزيائي الهولندي فان دير وولز، عام 1873م، بحساب حجم الجزيئات والقوى بينها، وبيّن أنّ سبب عدم تسييل الغازات الثابته بأنه ينبغي تبريد كلّ جزيء تحت درجة حرارة حرجة. وتوصّل لطريقة جديدة تمكّن من خلالها تسييل الأكسجين ثم تسييل النيتروجين ووصل لدرجة 200 درجة مئوية تحت الصفر، أي 73 درجة كلفن. ولم يتبقّى سوى غاز واحد من الغازات الثابتة ليسيل وهو الهيدروجين. تمكّن ديوار من تسييل الهيدروجين؛ آخر الغازات الثابتة التي ذكرها فاراداي، عند درجة حرارة 250 درجة مئوية تحت الصفر، أي 23 درجة كلفن.
اتّجهت الأنظار بعد ذلك للهيليوم وهو غاز خامل كان مكتشَفًا حديثًا ونجح أونيس في تسييل غاز الهيليوم عند درجة حرارة 268 مئوية تحت الصفر، أي عند درجات فوق الصفر المطلق، وحصل على جائزة نوبل على هذا الاكتشاف.
حالات للمادة تم اكتشافها أثناء محاولة الوصول للصفر المطلق:
الموصلية الفائقة:
في معمل لايدن بهولندا عام 1911م، قام فريق العالم أونيس بإجراء تجارب على موصلية المواد للكهرباء في درجات الحرارة المنخفضة، ولاحظ أنه عند حوالي 4 درجات كلفن انعدمت المقاومة تمامًا!
قبل هذا الاكتشاف كانت جميع الموادّ على الأرض يجب أن تكون لها مقاومة كهربائية حتى الموصلات. وأطلق أونيس على هذه الحالة “الموصلية الفائقة”. ولمعرفة أهمية المادة عند الموصلية الفائقة فإننا لو وضعنا قرصًا من هذه المادة فوق مجال كهرومغناطيسي في مسار دائري وتمّ دفعه فإنّ القرص يكتسب مجالًا مغناطيسيًا مشابهًا لقطبية المجال المغناطيسي للمغناطيس الثابت، وهذا يجعل القرص يتنافر ويرتفع سنتيمترات ويدور دون أن يتوقّف، وهذا الأمر يشبه القطار المغناطيسي في اليابان.

حفّز هذا الاكتشاف خيال العلماء لخلق هذه المادة لأن هذا من شأنه تحسين توليد الكهرباء ونقلها.
الميوعة الفائقة:
عندما يتمّ تبريد الهيليوم ونصل لدرجتين فوق الصفر المطلق يحدث تحول مثير. نجد أنّ الفقّاعات داخل السائل وعلى سطحه تتوقف تمامًا ويصبح راكدًا تمامًا. ويتحوّل الهيليوم السائل لمائع فائق. لهذا المائع خصائص غريبة؛ مثل القدرة على اختراق الكوب والتسرّب منه ويُطلق على هذا التدفّق “التدفّق المثالي.”

هذا المائع الفائق يتحدى الجاذبية، فمن الممكن لطبقة رقيقة منه تسلّق الجدران والهروب من الوعاء الذي يحويها وسبب ذلك أنّ المائع عديم اللزوجة تمامًا حتى أنه باستطاعته خلق نافورة عديمة الاحتكاك، كما في الصورة. وأحيانًا تصنّف هذه المادة أنها الحالة الخامسة للمادة.

وتوجد ظاهرة غريبة لهذا المائع الفائق؛ فلو أخذنا جزءًا من هذا المائع الفائق فإنّ الجزء الذي أخذناه يسعى للوصول مرة أخرى للعودة للمائع الأصلي.
مكثف بوز -آينشتاين:
في عام 1925م أرسل شابّ فيزيائي هندي يدعى “ساتيندرا بوز” ورقة بحثية لآينشتاين لم يستطع نشرها بنفسه. حاول بوز في هذه الورقة البحثية تطبيق الرياضيات الخاصة بالضوء على الذرات جميعًا. أدرك آينشتاين أهمية هذا العمل وقام ببعض الإضافات على الورقة البحثية وتوقّع أنه عند درجات الحرارة بالغة الانخفاض، أي فوق الصفر المطلق بقليل جدًّا، من الممكن استحداث نوع جديد من المادة يخضع لقوانين الكم، وهذه الحالة لن تكون صلبة أو سائلة أو غازية وتمّت تسميتها “مكثف بوز – آينشتاين.”
من الخصائص الغريبة في هذه المادة أنها لا تصبح الجزيئات مجرّد أجسام صلبة ولكنها تتحول لحزم موجية، وعند التبريد أكثر تزداد الأطوال الموجية لهذه الحزم ثمّ تتشابك وحينها لا يسلك النظام الجديد سلوك الجزيئات المفردة وتفقد الذرات هويتها (وتعتقد جميعها أنها موجودة بكلّ مكان) وتصبح جميعها في حالة كمومية مثل قطة شرودنجر، كما شرحنا سابقًا، أنه كلما قلّت درجة الحرارة تزداد الروابط بين الذرات وبالتالي تقترب ببعضها أكثر، وهذا ما يحدث في هذه المادة بالإضافة لتحولها للحزم الموجية والتشابك فتصبح الذرات وكأنها ذرة واحدة كبيرة، كما أنها تفقد طاقتها الحركية تقريبًا وتصبح ساكنة ومستقرة. وتعتبر هذه الحالة هي الحالة السادسة للمادة.

إعلان
